每日經濟新聞 2020-12-18 21:29:40
值得注意的是,雖然國內創新藥企業勢頭猛烈,但未來可能要面臨過度競爭的局面。過度競爭也就意味著要靠價格戰拼市場,一些技術路線較為落后的產品可能會在產品迭代中被淘汰。
每經記者 金喆 每經編輯 魏官紅

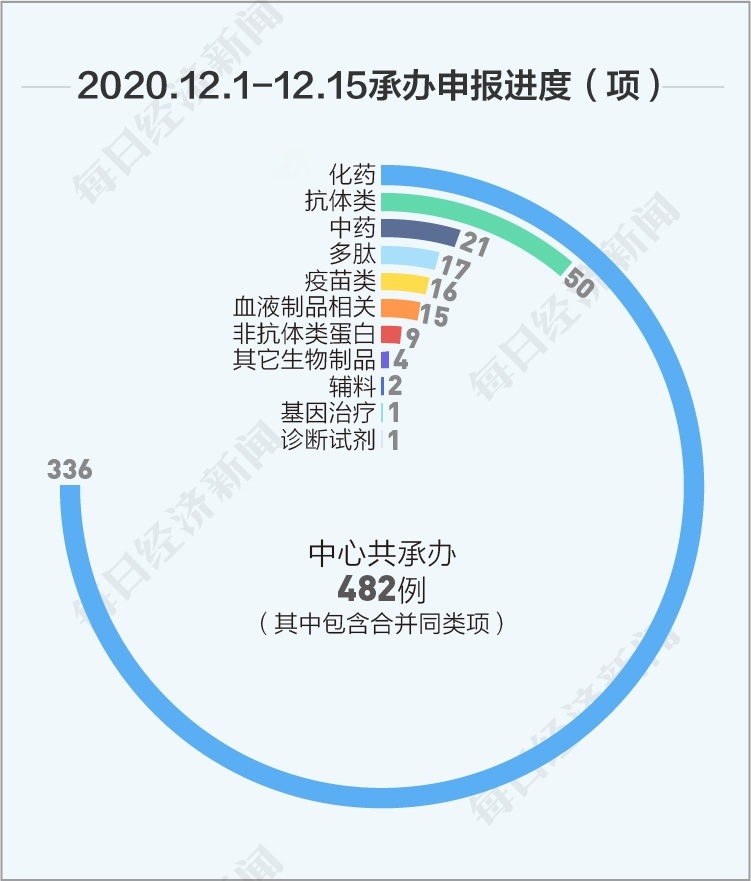
丁香園Insight數據庫援引國家藥品監督管理局藥品審評中心數據顯示,12月1日~12月15日,中心共承辦482例申報進度。其中,受理化藥申請336項,抗體類50項,中藥申請21項,多肽17項,疫苗類16項,血液制品相關15項,非抗體類蛋白9項,其它生物制品4項,輔料2項,基因治療1項,診斷試劑1項。
本階段醫藥行業最大熱點是2020年醫保談判,最熱門品種自然繞不開PD-1。2019年,信達生物PD-1抗體藥物降價近64%,全年費用降至約9.7萬元,成為唯一進醫保目錄的PD-1。今年前三季度,信達生物PD-1銷售額超過25億元,由此可見醫保的貢獻作用。
根據丁香園Insight數據庫,目前國內已有8個PD-1類產品上市,超過30種產品在研。今年的談判,參與者更多、籌碼也更多,最終哪家企業能進入醫保后的大市場,值得外界關注。
但激烈、甚至稱得上慘烈的價格競爭也給行業警示:雖然國內創新藥企業勢頭猛烈,但因彼此扎堆的靶點和適應癥差別不大,未來可能要面臨過度競爭的局面。而過度競爭也就意味著又要靠價格戰拼市場,一些技術路線較為落后的產品可能會在產品迭代中被淘汰。
1、2020年醫保談判結束,醫藥股普遍飄紅
去年醫保談判時“靈魂砍價”的場景歷歷在目,今年12月17日靴子落地后,醫藥股集體暴漲。實際上,每年一次的醫保談判已逐漸常態化,企業也越來越適應這種節奏,只有降價是硬招數。
本輪醫藥板塊強勢反彈,與談判降價效果比此前預估的要“溫和”有關。此前,行業預期降價幅度將在80%以上,甚至達到90%。但根據目前流出的消息,降價幅度均沒有此前預計的力度大,比如中成藥降幅約40%,PD-1降價幅度約80%。
根據過往經驗,進入醫保目錄對企業而言是利好,如果降價幅度低于預期的話,則是錦上添花。
興業證券醫藥小組發布的研報指出,回顧過去創新藥談判,競爭格局較好的品種和競爭相對激烈的品種,在通過談判納入醫保后,均能實現較快放量,給相應品種帶來彈性空間。
“我們以曲妥珠單抗(生物類似物,尚未獲批)和奧希替尼(競品于今年剛上市)為例。從PDB樣本醫院數據來看,其在通過談判納入醫保后均實現快速放量,極大地體現出納入醫保可以助推創新藥加速放量增長。”興業證券分析指出,納入醫保之前,雖然這些藥物具備較高的臨床價值,但因為價格相對較高而導致市場滲透率較低,進入醫保之后這些藥物的臨床使用率得到迅速提升。
從企業角度來說,新藥上市進入醫保的周期縮短,如果順利進入醫保則意味著能快速放量,潛在患者規模和競爭格局的“量價”博弈還可以考慮。經過多輪國家醫保談判,企業對基本流程及需要準備的資料亦心中有數,現在醫保調整周期基本明確,基本上一輪談判結束,就要開始著手次年上市產品的準備工作。
但我們仍需要分析PD-1上市后的激烈競爭情況,為創新藥下一步發展提供更明確的方向。
2018年6月,2款PD-1進口藥獲批,月費用約4萬元,同年12月,2款國產藥獲批,月費用降到約1.4萬元。2019年底醫保談判后,信達生物信迪利單抗醫保后年費用約2.9萬元。根據目前流出的消息,本次進入醫保的國產PD-1患者實際支付的年治療費用降至1.5萬元左右。不過,《每日經濟新聞》記者尚未從官方確認上述消息。
根據時間軸,藥物上市后難以避免價格競爭,創新藥研發難度大、資金需求高,如果扎堆在相同靶點,未來也可能跟PD-1的情況類似。廣東省肺癌研究所名譽所長吳一龍等人總結了中國國內抗腫瘤藥物的研發現狀:截至2020年1月,中國有821種正在研究的抗腫瘤藥物,其中包括404種me-too藥物和359種first-in-class藥物。
《每日經濟新聞》記者根據數據統計,當前國內最新藥物研發熱門靶點包括PD-1/PD-L1、CTLA-4、CAR-T、CD20、EGFR、TNF-α等,大多集中在腫瘤治療不同領域,并吸引了國內外企業的共同競爭。
2、恒瑞1類新藥氟唑帕利膠囊即將獲批,為首個國產
丁香園Insight數據庫顯示,12月3日,恒瑞醫藥1類新藥「氟唑帕利膠囊」上市申請進入行政審批階段,預計將在近日獲批,該藥是國內企業自主研發的首個PARP抑制劑,用于治療既往經過二線及以上化療的伴有BRCA1/2致病性或疑似致病性突變的復發性卵巢癌患者。
目前,全球共有4個PARP抑制劑上市。其中,奧拉帕利2018年在國內獲批上市,并在2019年醫保談判中降價61.8%進入醫保乙類目錄,醫保支付標準為169.00元(150mg/片),尼拉帕利2019年在國內獲批上市。據Insight數據庫,奧拉帕利全球銷售額連年增長,在2019年已達到16.42億美元,同比增長94.8%,市場潛力巨大。
恒瑞已針對氟唑帕利開展了26項臨床,適應癥涉及小細胞肺癌、實體瘤、復發轉移三陰乳腺癌、前列腺癌、復發性卵巢癌、晚期胃癌等。其中,15項臨床尚在進行中,包括4項III期臨床。另外,國內已有多個企業布局PARP抑制劑,10個企業已進入臨床階段。
3、諾誠健華BTK抑制劑奧布替尼片即將獲批上市
丁香園Insight數據庫顯示,近日,諾誠健華(09969,HK)奧布替尼片(orelabrutinib)在國內的注冊申請進入“在審批”階段,有望于近期獲得批準,用于單藥治療既往至少接受過一種治療的慢性淋巴細胞白血病/小淋巴細胞淋巴瘤(CLL/SLL)以及既往至少接受過一種治療的套細胞淋巴瘤(MCL)。
這意味著奧布替尼將成為繼伊布替尼、澤布替尼后,國內第三個獲批上市的BTK抑制劑。
根據諾誠健華早前發布的臨床研究數據,奧布替尼治療復發難治性CLL/SLL患者的2期研究中,患者的總體客觀緩解率(ORR)高達88.8%。在2020年美國血液學會(ASH)年會上,諾誠健華公布的2期研究更新數據顯示:奧布替尼單藥治療復發/難治CLL/SLL中國患者,具有較高的完全緩解率(CR)、持久的反應和改善的安全性。
此外,諾誠健華還在探索奧布替尼治療復發難治性邊緣區淋巴瘤(MZL)、中樞神經系統白血病(CNSL)、華氏巨球蛋白血癥(WM)、濾泡性淋巴瘤(FL)、多發性硬化(MS)等適應癥的治療效果。這意味著,未來奧布替尼有望惠及更多的患者。
1、本期首次注冊上市的品種有10個(如下圖所示)
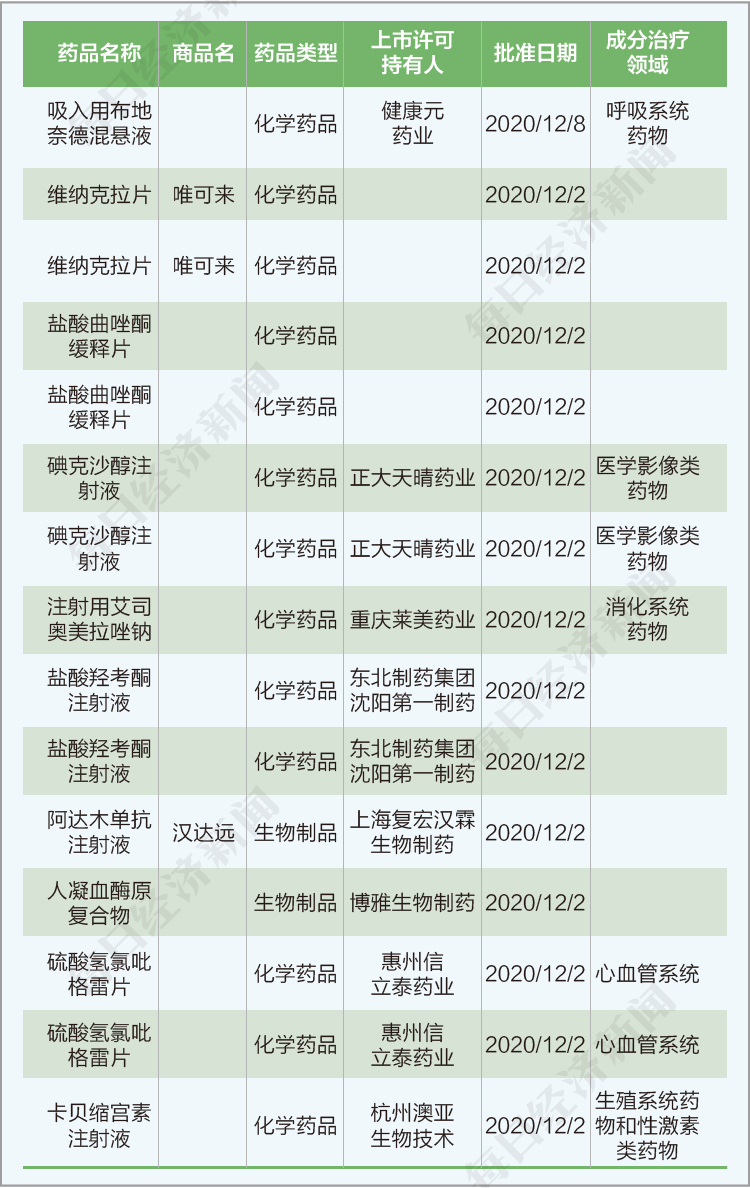
2、本階段申報的項目中,化藥仿制藥100項,化藥新藥/原研藥111項,生物制品新藥/原研藥62項,化藥改良型新藥6項,非原研/類似藥生物制品26項,生物制品改良型新藥3項,生物制品類似藥1項,暫時不明15項。
按成分治療領域排名,前五位是抗腫瘤藥物(66項),抗感染藥物(56項),免疫系統藥物(53項),神經系統藥物(40項)和心血管系統藥物(35項)。

本階段無藥物納入優先審評審批品種。
本階段有16個創新藥品種開展臨床試驗。
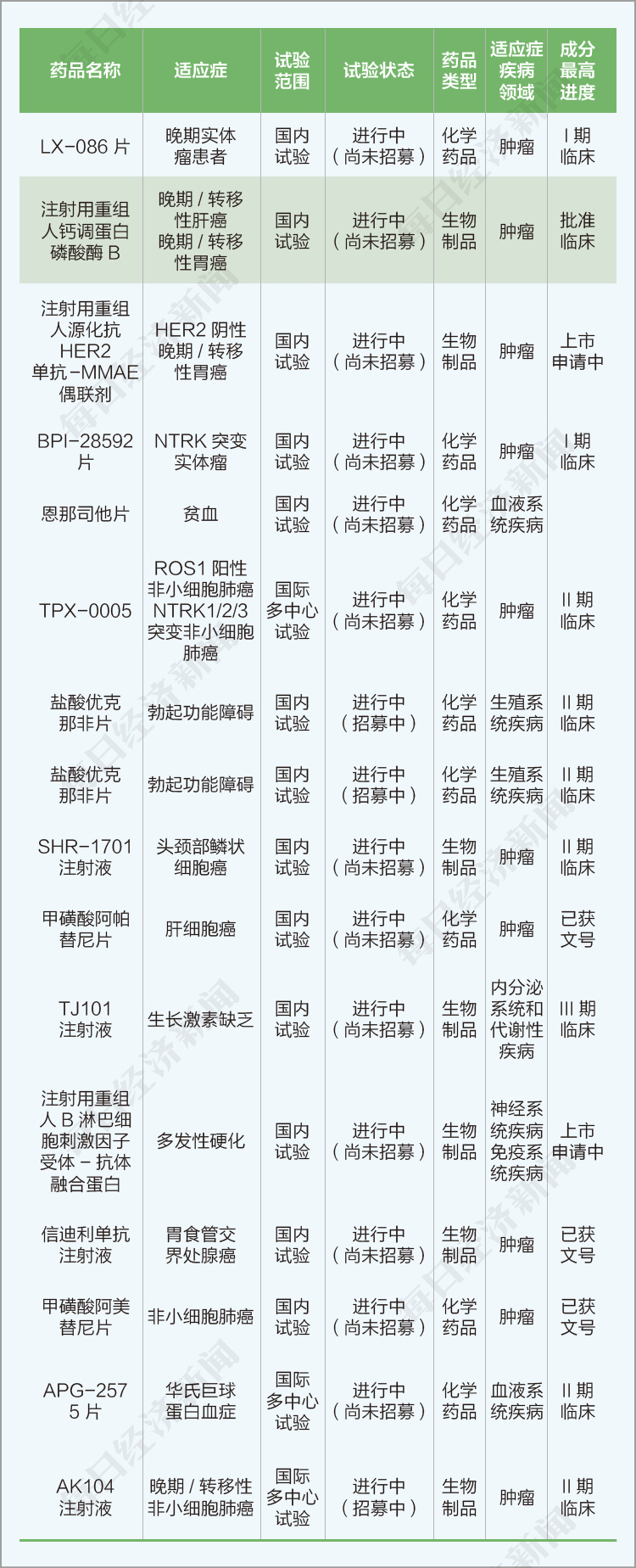
3、本期共有一類注冊新藥臨床申請15個(不含補充申請)。
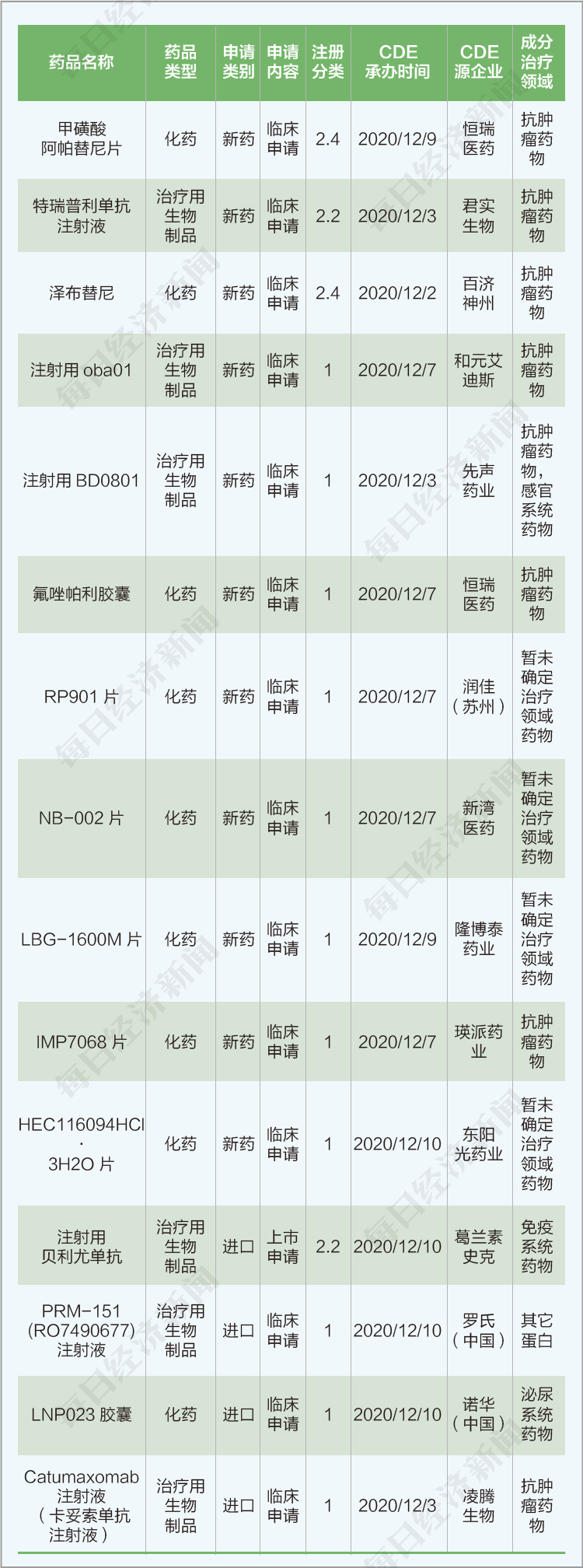
“每經數說丨新藥研發”由每日經濟新聞編制,每半月發布一次。為避免我們資料收集過程中出現遺漏,請創新藥研發企業及時將創新藥研發進展通報給我們,以便我們及時計入指數并計算權重。
聯絡郵箱:jinzhe@nbd.com.cn
封面圖片來源:攝圖網
如需轉載請與《每日經濟新聞》報社聯系。
未經《每日經濟新聞》報社授權,嚴禁轉載或鏡像,違者必究。
讀者熱線:4008890008
特別提醒:如果我們使用了您的圖片,請作者與本站聯系索取稿酬。如您不希望作品出現在本站,可聯系我們要求撤下您的作品。
歡迎關注每日經濟新聞APP
